| Teori Kinetik Gas Fisika Kelas 1 > Teori Kinetik Zat | 284 | ||||
Teori kinetik zat membicarakan sifat zat dipandang dari sudut momentum. Peninjauan teori ini bukan pada kelakuan sebuah partikel, tetapi diutamakan pada sifat zat secara keseluruhan sebagai hasil rata-rata kelakuan partikel-partikel zat tersebut. SIFAT GAS UMUM
PERSAMAAN GAS IDEAL DAN TEKANAN (P) GAS IDEAL P V = n R T = N K T n = N/No T = suhu (ºK) R = K . No = 8,31 )/mol. ºK N = jumlah pertikel P = (2N / 3V) . Ek ® T = 2Ek/3K V = volume (m3) n = jumlah molekul gas K = konstanta Boltzman = 1,38 x 10-23 J/ºK No = bilangan Avogadro = 6,023 x 1023/mol ENERGI TOTAL (U) DAN KECEPATAN (v) GAS IDEAL Ek = 3KT/2 U = N Ek = 3NKT/2 v = Ö(3 K T/m) = Ö(3P/r) dengan: Ek = energi kinetik rata-rata tiap partikel gas ideal U = energi dalam gas ideal = energi total gas ideal v = kecepatan rata-rata partikel gas ideal m = massa satu mol gas p = massa jenis gas ideal Jadi dari persamaan gas ideal dapat diambil kesimpulan:
Dari persarnaan gas ideal PV = nRT, dapat di jabarkan:
1. Berapakah kecepatan rata-rata dari partikel-partikel suatu gas dalam keadaan normal, jika massa jenis gas 100 kg/m3 dan tekanannya 1,2.105 N/m2? Jawab: PV = 2/3 Ek PV = 2/3 . 1/2 . m v2 = 1/3 m v2 v2 = (3PV)/m = (3 P)/(m/V) = 3P/r v = Ö3P/r = Ö3.1,2.105/100 = 60 m/det 2. Suatu gas tekanannya 15 atm dan volumenya 25 cm3 memenuhi persamaan PV - RT. Bila tekanan gas berubah 1/10 atm tiap menit secara isotermal. Hitunglah perubahan volume gas tiap menit? Jawab: Persamaan PV = RT jelas untuk gas ideal dengan jumlah mol gas n = 1. Jadi kita ubah persamaan tersebut menjadi: P DV + V DP = R DT (cara differensial parsial) 15 . DV + 25. 1/10 = R . 0 ® AV = -25 /15.10 = -1/6 cm3/menit Jadi perubahan volume gas tiap menit adalah 1/6 cm3,dimana tanda (-) menyatakan gas menerima usaha dari luar (dari sekelilingnya). | |||||
Tampilkan postingan dengan label fisika. Tampilkan semua postingan
Tampilkan postingan dengan label fisika. Tampilkan semua postingan
Sabtu, 26 Maret 2011
kinetik gas
gerak harmonik sederhana
Gaya Pemulih pada Gerak Harmonik SederhanaGaya Pemulih pada Pegask = konstanta pegas (N/m)y = simpangan (m)Gaya Pemulih pada Ayunan Bandul Sederhanam = massa benda (kg)g = percepatan gravitasi (m/s2)θsin mgF= vektor)(notasi skalar) (notasi ykFkyFvv−==Periode dan FrekuensiPeriode adalah waktu yg diperlukan untuk melakukan satu kali gerak bolak-balik.Frekuensi adalah banyaknya getaran yang dilakukan dalam waktu 1 detik.Untuk pegasyg memiliki konstanta gaya k yg bergetar karena adanya beban bermassa m, periode getarnya adalahSedangkan pada ayunan bandul sederhana, jika panjang tali adalah l, maka periodenya adalahkmTπ2=fTTf1atau 1==glTπ2=Simpangan, Kecepatan, PercepatanSimpangan Gerak Harmonik Sederhanay = simpangan (m)A = amplitudo (m)ω= kecepatan sudut (rad/s)f = frekuensi (Hz)t = waktu tempuh (s)Jika pada saat awal benda pada posisi θ0, makaBesar sudut (ωt+θ0) disebut sudut fase (θ), sehinggaφdisebut fase getaran dan Δφdisebut beda fase.πftAωtAy2sin sin ==)2(sin )(sin 00θθ+=+=πftAωtAy002θθθ+=+=TtπωtTttπTtππTtπ1212002222−=−=Δ+==⎟⎠⎞⎜⎝⎛+=ϕϕϕθϕϕθθKecepatan Gerak Harmonik SederhanaUntuk benda yg pada saat awal θ0= 0, maka kecepatannya adalahNilai kecepatan v akan maksimum pada saat cos ωt = 1, sehinggakecepatan maksimumnya adalahKecepatan benda di sembarang posisi y adalahωtAωtAdtddtdyv cos )sin (ω===Avmω=22yAvy−=ω
Kamis, 24 Maret 2011
termodinamika
Termodinamika adalah kajian tentang kalor (panas) yang berpindah. Dalam termodinamika kamu akan banyak membahas tentang sistem dan lingkungan. Kumpulan benda-benda yang sedang ditinjau disebut sistem, sedangkan semua yang berada di sekeliling (di luar) sistem disebut lingkungan.
Usaha Luar
Usaha luar dilakukan oleh sistem, jika kalor ditambahkan (dipanaskan) atau kalor dikurangi (didinginkan) terhadap sistem. Jika kalor diterapkan kepada gas yang menyebabkan perubahan volume gas, usaha luar akan dilakukan oleh gas tersebut. Usaha yang dilakukan oleh gas ketika volume berubah dari volume awal V1 menjadi volume akhir V2 pada tekanan p konstan dinyatakan sebagai hasil kali tekanan dengan perubahan volumenya.
W = p∆V= p(V2 – V1)
Secara umum, usaha dapat dinyatakan sebagai integral tekanan terhadap perubahan volume yang ditulis sebagai
 Gas dikatakan melakukan usaha apabila volume gas bertambah besar (atau mengembang) dan V2 > V1. sebaliknya, gas dikatakan menerima usaha (atau usaha dilakukan terhadap gas) apabila volume gas mengecil atau V2 < V1 dan usaha gas bernilai negatif.
Gas dikatakan melakukan usaha apabila volume gas bertambah besar (atau mengembang) dan V2 > V1. sebaliknya, gas dikatakan menerima usaha (atau usaha dilakukan terhadap gas) apabila volume gas mengecil atau V2 < V1 dan usaha gas bernilai negatif.Energi Dalam
Suatu gas yang berada dalam suhu tertentu dikatakan memiliki energi dalam. Energi dalam gas berkaitan dengan suhu gas tersebut dan merupakan sifat mikroskopik gas tersebut. Meskipun gas tidak melakukan atau menerima usaha, gas tersebut dapat memiliki energi yang tidak tampak tetapi terkandung dalam gas tersebut yang hanya dapat ditinjau secara mikroskopik.
Berdasarkan teori kinetik gas, gas terdiri atas partikel-partikel yang berada dalam keadaan gerak yang acak. Gerakan partikel ini disebabkan energi kinetik rata-rata dari seluruh partikel yang bergerak. Energi kinetik ini berkaitan dengan suhu mutlak gas. Jadi, energi dalam dapat ditinjau sebagai jumlah keseluruhan energi kinetik dan potensial yang terkandung dan dimiliki oleh partikel-partikel di dalam gas tersebut dalam skala mikroskopik. Dan, energi dalam gas sebanding dengan suhu mutlak gas. Oleh karena itu, perubahan suhu gas akan menyebabkan perubahan energi dalam gas. Secara matematis, perubahan energi dalam gas dinyatakan sebagai
untuk gas monoatomik
untuk gas diatomik
Dimana ∆U adalah perubahan energi dalam gas, n adalah jumlah mol gas, R adalah konstanta umum gas (R = 8,31 J mol−1 K−1, dan ∆T adalah perubahan suhu gas (dalam kelvin).
Hukum I Termodinamika
Jika kalor diberikan kepada sistem, volume dan suhu sistem akan bertambah (sistem akan terlihat mengembang dan bertambah panas). Sebaliknya, jika kalor diambil dari sistem, volume dan suhu sistem akan berkurang (sistem tampak mengerut dan terasa lebih dingin). Prinsip ini merupakan hukum alam yang penting dan salah satu bentuk dari hukum kekekalan energi.
Gambar
Sistem yang mengalami perubahan volume akan melakukan usaha dan sistem yang mengalami perubahan suhu akan mengalami perubahan energi dalam. Jadi, kalor yang diberikan kepada sistem akan menyebabkan sistem melakukan usaha dan mengalami perubahan energi dalam. Prinsip ini dikenal sebagai hukum kekekalan energi dalam termodinamika atau disebut hukum I termodinamika. Secara matematis, hukum I termodinamika dituliskan sebagai
Q = W + ∆U
Dimana Q adalah kalor, W adalah usaha, dan ∆U adalah perubahan energi dalam. Secara sederhana, hukum I termodinamika dapat dinyatakan sebagai berikut.
Jika suatu benda (misalnya krupuk) dipanaskan (atau digoreng) yang berarti diberi kalor Q, benda (krupuk) akan mengembang atau bertambah volumenya yang berarti melakukan usaha W dan benda (krupuk) akan bertambah panas (coba aja dipegang, pasti panas deh!) yang berarti mengalami perubahan energi dalam ∆U.
Proses Isotermik
Suatu sistem dapat mengalami proses termodinamika dimana terjadi perubahan-perubahan di dalam sistem tersebut. Jika proses yang terjadi berlangsung dalam suhu konstan, proses ini dinamakan proses isotermik. Karena berlangsung dalam suhu konstan, tidak terjadi perubahan energi dalam (∆U = 0) dan berdasarkan hukum I termodinamika kalor yang diberikan sama dengan usaha yang dilakukan sistem (Q = W).
Proses isotermik dapat digambarkan dalam grafik p – V di bawah ini. Usaha yang dilakukan sistem dan kalor dapat dinyatakan sebagai

Proses Isokhorik
Jika gas melakukan proses termodinamika dalam volume yang konstan, gas dikatakan melakukan proses isokhorik. Karena gas berada dalam volume konstan (∆V = 0), gas tidak melakukan usaha (W = 0) dan kalor yang diberikan sama dengan perubahan energi dalamnya. Kalor di sini dapat dinyatakan sebagai kalor gas pada volume konstan QV.
QV = ∆U
Proses Isobarik
Jika gas melakukan proses termodinamika dengan menjaga tekanan tetap konstan, gas dikatakan melakukan proses isobarik. Karena gas berada dalam tekanan konstan, gas melakukan usaha (W = p∆V). Kalor di sini dapat dinyatakan sebagai kalor gas pada tekanan konstan Qp. Berdasarkan hukum I termodinamika, pada proses isobarik berlaku
QV =∆U
Dari sini usaha gas dapat dinyatakan sebagai
W = Qp − QV
Jadi, usaha yang dilakukan oleh gas (W) dapat dinyatakan sebagai selisih energi (kalor) yang diserap gas pada tekanan konstan (Qp) dengan energi (kalor) yang diserap gas pada volume konstan (QV).

Proses Adiabatik
Dalam proses adiabatik tidak ada kalor yang masuk (diserap) ataupun keluar (dilepaskan) oleh sistem (Q = 0). Dengan demikian, usaha yang dilakukan gas sama dengan perubahan energi dalamnya (W = ∆U).
Jika suatu sistem berisi gas yang mula-mula mempunyai tekanan dan volume masing-masing p1 dan V1 mengalami proses adiabatik sehingga tekanan dan volume gas berubah menjadi p2 dan V2, usaha yang dilakukan gas dapat dinyatakan sebagai

Proses adiabatik dapat digambarkan dalam grafik p – V dengan bentuk kurva yang mirip dengan grafik p – V pada proses isotermik namun dengan kelengkungan yang lebih curam.
teori kinetik gas
| |||||||||||||
kesetimbangan benda tegar
Telah dikatakan sebelumnya bahwa suatu benda tegar dapat mengalami gerak translasi (gerak lurus) dan gerak rotasi. Benda tegar akan melakukan gerak translasi apabila gaya yang diberikan pada benda tepat mengenai suatu titik yang yang disebut titik berat.
Mari kita tinjau suatu benda tegar, misalnya tongkat pemukul kasti, kemudian kita lempar sambil sedikit berputar. Kalau kita perhatikan secara aeksama, gerakan tongkat pemukul tadi dapat kita gambarkan seperti membentuk suatu lintasan dari gerak translasi yang sedang dijalani dimana pada kasus ini lintasannya berbentuk parabola. Tongkat ini memang berputar pada porosnya, yaitu tepat di titik beratnya. Dan, secara keseluruhan benda bergerak dalam lintasan parabola. Lintasan ini merupakan lintasan dari posisi titik berat benda tersebut.
Demikian halnya seorang peloncat indah yang sedang terjun ke kolam renang. Dia melakukan gerak berputar saat terjun. sebagaimana tongkat pada contoh di atas, peloncat indah itu juga menjalani gerak parabola yang bisa dilihat dari lintasan titik beratnya. Perhatikan gambar berikut ini.
Cara untuk mengetahui letak titik berat suatu benda tegar akan menjadi mudah untuk benda-benda yang memiliki simetri tertentu, misalnya segitiga, kubus, balok, bujur sangkar, bola dan lain-lain. Yaitu d sama dengan letak sumbu simetrinya. Hal ini jelas terlihat pada contoh diatas bahwa letak titik berat sama dengan sumbu rotasi yang tidak lain adalah sumbu simetrinya.
Possibly related posts: (automatically generated)
Jumat, 18 Maret 2011
hubungan dasar fluida
Seperti halnya model matematika pada umumnya, mekanika fluida membuat beberapa asumsi dasar berkaitan dengan studi yang dilakukan. Asumsi-asumsi ini kemudian diterjemahkan ke dalam persamaan-persamaan matematis yang harus dipenuhi bila asumsi-asumsi yang telah dibuat berlaku.
Mekanika fluida mengasumsikan bahwa semua fluida mengikuti:
Selain itu, kadang-kadang viskositas dari suatu fluida dapat diasumsikan bernilai nol (fluida tidak viskos). Terkadang gas juga dapat diasumsikan bersifat tidak viskos. Jika suatu fluida bersifat viskos dan alirannya ditampung dalam suatu cara (seperti dalam pipa), maka aliran pada batas sistemnya mempunyai kecepatan nol. Untuk fluida yang viskos, jika batas sistemnya tidak berpori, maka gaya geser antara fluida dengan batas sistem akan memberikan resultan kecepatan nol pada batas fluida.
Hipotesis kontinum pada dasarnya hanyalah pendekatan. Sebagai akibatnya, asumsi hipotesis kontinum dapat memberikan hasil dengan tingkat akurasi yang tidak diinginkan. Namun demikian, bila kondisi benar, hipotesis kontinum menghasilkan hasil yang sangat akurat.
Masalah akurasi ini biasa dipecahkan menggunakan mekanika statistik. Untuk menentukan perlu menggunakan dinamika fluida konvensial atau mekanika statistik, angka Knudsen permasalahan harus dievaluasi. Angka Knudsen didefinisikan sebagai rasio dari rata-rata panjang jalur bebas molekular terhadap suatu skala panjang fisik representatif tertentu. Skala panjang ini dapat berupa radius suatu benda dalam suatu fluida. Secara sederhana, angka Knudsen adalah berapa kali panjang diameter suatu partikel akan bergerak sebelum menabrak partikel lain.
Persamaan Navier-Stokes memiliki bentuk persamaan diferensial yang menerangkan pergerakan dari suatu fluida. Persaman seperti ini menggambarkan hubungan laju perubahan suatu variabel terhadap variabel lain. Sebagai contoh, persamaan Navier-Stokes untuk suatu fluida ideal dengan viskositas bernilai nol akan menghasilkan hubungan yang proposional antara percepatan (laju perubahan kecepatan) dan derivatif tekanan internal.
Untuk mendapatkan hasil dari suatu permasalahan fisika menggunakan persamaan Navier-Stokes, perlu digunakan ilmu kalkulus. Secara praktis, hanya kasus-kasus aliran sederhana yang dapat dipecahkan dengan cara ini. Kasus-kasus ini biasanya melibatkan aliran non-turbulen dan tunak (aliran yang tidak berubah terhadap waktu) yang memiliki nilai bilangan Reynold kecil.
Untuk kasus-kasus yang kompleks, seperti sistem udara global seperti El Niño atau daya angkat udara pada sayap, penyelesaian persamaan Navier-Stokes hingga saat ini hanya mampu diperoleh dengan bantuan komputer. Kasus-kasus mekanika fluida yang membutuhkan penyelesaian berbantuan komputer dipelajari dalam bidang ilmu tersendiri yaitu mekanika fluida komputasional
 adalah tensor yang simetris kecuali bila fluida tersusun dari derajat kebebasan yang berputar seperti vorteks. Secara umum, (dalam tiga dimensi)
adalah tensor yang simetris kecuali bila fluida tersusun dari derajat kebebasan yang berputar seperti vorteks. Secara umum, (dalam tiga dimensi)  memiliki bentuk persamaan:
memiliki bentuk persamaan:
Sebaliknya, bila fluida non-Newtonian diaduk, akan tersisa suatu "lubang". Lubang ini akan terisi seiring dengan berjalannya waktu. Sifat seperti ini dapat teramati pada material-material seperti puding. Peristiwa lain yang terjadi saat fluida non-Newtonian diaduk adalah penurunan viskositas yang menyebabkan fluida tampak "lebih tipis" (dapat dilihat pada cat). Ada banyak tipe fluida non-Newtonian yang kesemuanya memiliki properti tertentu yang berubah pada keadaan tertentu.
Mekanika fluida mengasumsikan bahwa semua fluida mengikuti:
- Hukum kekekalan massa
- Hukum kekekalan momentum
- Hipotesis kontinum, yang dijelaskan di bagian selanjutnya.
Selain itu, kadang-kadang viskositas dari suatu fluida dapat diasumsikan bernilai nol (fluida tidak viskos). Terkadang gas juga dapat diasumsikan bersifat tidak viskos. Jika suatu fluida bersifat viskos dan alirannya ditampung dalam suatu cara (seperti dalam pipa), maka aliran pada batas sistemnya mempunyai kecepatan nol. Untuk fluida yang viskos, jika batas sistemnya tidak berpori, maka gaya geser antara fluida dengan batas sistem akan memberikan resultan kecepatan nol pada batas fluida.
[sunting] Hipotesis kontinum
Fluida disusun oleh molekul-molekul yang bertabrakan satu sama lain. Namun demikian, asumsi kontinum menganggap fluida bersifat kontinu. Dengan kata lain, properti seperti densitas, tekanan, temperatur, dan kecepatan dianggap terdefinisi pada titik-titik yang sangat kecil yang mendefinisikan REV (‘’Reference Element of Volume’’) pada orde geometris jarak antara molekul-molekul yang berlawanan di fluida. Properti tiap titik diasumsikan berbeda dan dirata-ratakan dalam REV. Dengan cara ini, kenyataan bahwa fluida terdiri dari molekul diskrit diabaikan.Hipotesis kontinum pada dasarnya hanyalah pendekatan. Sebagai akibatnya, asumsi hipotesis kontinum dapat memberikan hasil dengan tingkat akurasi yang tidak diinginkan. Namun demikian, bila kondisi benar, hipotesis kontinum menghasilkan hasil yang sangat akurat.
Masalah akurasi ini biasa dipecahkan menggunakan mekanika statistik. Untuk menentukan perlu menggunakan dinamika fluida konvensial atau mekanika statistik, angka Knudsen permasalahan harus dievaluasi. Angka Knudsen didefinisikan sebagai rasio dari rata-rata panjang jalur bebas molekular terhadap suatu skala panjang fisik representatif tertentu. Skala panjang ini dapat berupa radius suatu benda dalam suatu fluida. Secara sederhana, angka Knudsen adalah berapa kali panjang diameter suatu partikel akan bergerak sebelum menabrak partikel lain.
[sunting] Persamaan Navier-Stokes
Persamaan Navier-Stokes (dinamakan dari Claude-Louis Navier dan George Gabriel Stokes) adalah serangkaian persamaan yang menjelaskan pergerakan dari suatu fluida seperti cairan dan gas. Persamaan-persamaan ini menyatakan bahwa perubahan dalam momentum (percepatan) partikel-partikel fluida bergantung hanya kepada gaya viskos internal (mirip dengan gaya friksi) dan gaya viskos tekanan eksternal yang bekerja pada fluida. Oleh karena itu, persamaan Navier-Stokes menjelaskan kesetimbangan gaya-gaya yang bekerja pada fluida.Persamaan Navier-Stokes memiliki bentuk persamaan diferensial yang menerangkan pergerakan dari suatu fluida. Persaman seperti ini menggambarkan hubungan laju perubahan suatu variabel terhadap variabel lain. Sebagai contoh, persamaan Navier-Stokes untuk suatu fluida ideal dengan viskositas bernilai nol akan menghasilkan hubungan yang proposional antara percepatan (laju perubahan kecepatan) dan derivatif tekanan internal.
Untuk mendapatkan hasil dari suatu permasalahan fisika menggunakan persamaan Navier-Stokes, perlu digunakan ilmu kalkulus. Secara praktis, hanya kasus-kasus aliran sederhana yang dapat dipecahkan dengan cara ini. Kasus-kasus ini biasanya melibatkan aliran non-turbulen dan tunak (aliran yang tidak berubah terhadap waktu) yang memiliki nilai bilangan Reynold kecil.
Untuk kasus-kasus yang kompleks, seperti sistem udara global seperti El Niño atau daya angkat udara pada sayap, penyelesaian persamaan Navier-Stokes hingga saat ini hanya mampu diperoleh dengan bantuan komputer. Kasus-kasus mekanika fluida yang membutuhkan penyelesaian berbantuan komputer dipelajari dalam bidang ilmu tersendiri yaitu mekanika fluida komputasional
[sunting] Bentuk umum persamaan
Bentuk umum persamaan Navier-Stokes untuk kekekalan momentum adalah :- ρ adalah densitas fluida,
 adalah derivatif substantif (dikenal juga dengan istilah derivatif dari material)
adalah derivatif substantif (dikenal juga dengan istilah derivatif dari material)
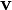 adalah vektor kecepatan,
adalah vektor kecepatan,- f adalah vektor gaya benda, dan
 adalah tensor yang menyatakan gaya-gaya permukaan yang bekerja pada partikel fluida.
adalah tensor yang menyatakan gaya-gaya permukaan yang bekerja pada partikel fluida.
 adalah tensor yang simetris kecuali bila fluida tersusun dari derajat kebebasan yang berputar seperti vorteks. Secara umum, (dalam tiga dimensi)
adalah tensor yang simetris kecuali bila fluida tersusun dari derajat kebebasan yang berputar seperti vorteks. Secara umum, (dalam tiga dimensi)  memiliki bentuk persamaan:
memiliki bentuk persamaan:- σ adalah tegangan normal, dan
- τ adalah tegangan tangensial (tegangan geser).
[sunting] Fluida Newtonian vs. non-Newtonian
Sebuah Fluida Newtonian (dinamakan dari Isaac Newton) didefinisikan sebagai fluida yang tegangan gesernya berbanding lurus secara linier dengan gradien kecepatan pada arah tegak lurus dengan bidang geser. Definisi ini memiliki arti bahwa fluida newtonian akan mengalir terus tanpa dipengaruhi gaya-gaya yang bekerja pada fluida. Sebagai contoh, air adalah fluida Newtonian karena air memiliki properti fluida sekalipun pada keadaan diaduk.Sebaliknya, bila fluida non-Newtonian diaduk, akan tersisa suatu "lubang". Lubang ini akan terisi seiring dengan berjalannya waktu. Sifat seperti ini dapat teramati pada material-material seperti puding. Peristiwa lain yang terjadi saat fluida non-Newtonian diaduk adalah penurunan viskositas yang menyebabkan fluida tampak "lebih tipis" (dapat dilihat pada cat). Ada banyak tipe fluida non-Newtonian yang kesemuanya memiliki properti tertentu yang berubah pada keadaan tertentu.
[sunting] Persamaan pada fluida Newtonian
Konstanta yang menghubungkan tegangan geser dan gradien kecepatan secara linier dikenal dengan istilah viskositas. Persamaan yang menggambarkan perlakuan fluida Newtonian adalah:- τ adalah tegangan geser yang dihasilkan oleh fluida
- μ adalah viskositas fluida-sebuah konstanta proporsionalitas
 adalah gradien kecepatan yang tegak lurus dengan arah geseran
adalah gradien kecepatan yang tegak lurus dengan arah geseran
- τij adalah tegangan geser pada bidang ith dengan arah jth
- vi adalah kecepatan pada arah ith
- xj adalah koordinat berarah jth
Langganan:
Komentar (Atom)